Page 45 - 9. Sınıf Kimya Öğretmenin Ders Notları (Hızlı)
P. 45
ATOM VE PERİYODİK SİSTEM 43
ATOMLARIN KATMAN ELEKTRON DAĞILIMI
F Bir atomda “n” gibi bir değer ile gösterilen en fazla 7 katman (yörünge, enerji düzeyi)
vardır.
F Katman (n), çekirdeğe en yakın olandan itibaren 1, 2, 3, 4... gibi tam sayılarla veya K,
L, M, N... gibi harflerle gösterilir.
F Her katmanda belirli sayıda elektron bulunabilir ve bir elektron bu katmanlardan sa-
dece birinde bulunabilir.
EDİTÖR YAYINEVİ
F Nötr bir atomun katman elektron dağılımı atom numarasına göre yapılır.
F Periyodik tablodaki ilk 20 element için bulunabilecek en fazla elektron sayıları aşa-
ğıda verilmiştir.
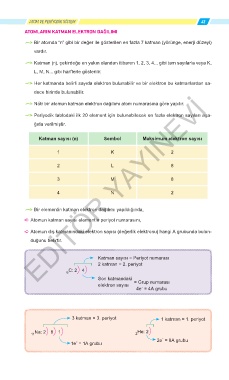
Katman sayısı (n) Sembol Maksimum elektron sayısı
1 K 2
2 L 8
3 M 8
4 N 2
F Bir elementin katman elektron dağılımı yapıldığında,
➪ Atomun katman sayısı elementin periyot numarasını,
➪ Atomun dış katmanındaki elektron sayısı (değerlik elektronu) hangi A grubunda bulun-
duğunu belirtir.
Katman sayısı = Periyot numarası
2 katman = 2. periyot
C: 2 4
6
Son katmandaki
elektron sayısı = Grup numarası
-
4e = 4A grubu
3 katman = 3. periyot 1 katman = 1. periyot
Na: 2 8 1 He: 2
11 2 -
-
1e = 1A grubu 2e = 8A grubu